医械资讯周刊 | 2024年9月第四期
医械资讯周刊 | 2024年9月第四期,本期要闻:颅内动脉瘤CT血管造影图像辅助检测软件获批上市,浙江省药品监督管理局关于第二类医疗器械注册电子申报和发放电子注册证的公告,上海市第二类创新医疗器械特别审查申请审查结果公示,广东省药品监督管理局关于同意东华至高通信技术有限公司等10家注册人主动注销《医疗器械注册证》的通告(2024年第105号)...
1、颅内动脉瘤CT血管造影图像辅助检测软件获批上市
近日,国家药品监督管理局批准了上海联影智能医疗科技有限公司的“颅内动脉瘤CT血管造影图像辅助检测软件”创新产品注册申请。
该产品由软件安装程序和授权文件组成,功能模块包括浏览器端、服务器端,用于头颈动脉CT血管造影图像的显示、处理、测量和分析,可对颅内3mm及以上动脉瘤进行辅助检测。
该产品采用基于深度学习的头颈血管分割分段技术和多尺度动脉瘤检测技术,有效提高了颅内动脉瘤的诊断准确性和效率,对提升患者生存率具有重要意义。
2、浙江省药品监督管理局关于第二类医疗器械注册电子申报和发放电子注册证的公告
经过一年试运行,浙江省医疗器械注册电子申报系统(以下简称浙械eRPS系统)已满足第二类医疗器械注册电子申报和发放电子注册证的条件,现就有关事项公告如下:
一、自2024年10月1日起,浙江省第二类医疗器械(含体外诊断试剂)产品注册、变更注册、延续注册、变更备案以及第二类医疗器械说明书变更备案通过浙江政务服务网电子申报,申请人无需再提交纸质资料。
二、自2024年10月1日起,浙江省第二类医疗器械(含体外诊断试剂)产品注册、变更注册、延续注册、变更备案所核发的医疗器械注册证及变更批件,采用电子注册证形式发放。电子注册证与纸质注册证具有同等法律效力,同时具备即时送达、短信提醒、扫码查询等功能。注册申请人通过浙江省药品监督管理局网站用户中心登录,即可在电子证照栏目下载所取得的医疗器械电子注册证。
三、涉及电子注册证获取、使用等相关问题解答可查看“浙江药闻”公众号相关链接https://mp.weixin.qq.com/s/FBDG_xbswPUxbDgSy9nCig,也可通过电话咨询。详细联系方式请见原文链接。
3、上海市第二类创新医疗器械特别审查申请审查结果公示(2024年第6号)
依据《上海市第二类创新医疗器械特别审查程序》要求,上海市药品监督管理局组织有关专家对本市第二类创新医疗器械特别审查申请进行了审查,拟同意以下申请项目进入特别审查程序,现予以公示。
产品名称:血细胞分析系统(含血细胞分析仪及血红蛋白/白细胞检测卡)
申请人:上海宜晟生物科技有限公司
公示时间:2024年9月24日至2024年10月11日
公示期内,任何单位和个人有异议的,可填写《第二类创新医疗器械特别审查异议表》,并通过邮寄或电子邮件的方式送达上海市药品监督管理局医疗器械创新审查服务办公室。联系方式详见原文链接。
4、上海市药品监督管理局关于对本市2024年医疗器械临床试验监督检查情况的通报
上海市药品监督管理局于2024年3月至8月,组织开展2024年医疗器械临床试验机构备案后监督检查和临床试验项目监督抽查。本次临床试验机构检查内容包括机构部分和专业部分共16个环节96个检查项目,共出动188人次,覆盖全市43家临床试验机构,检查结果为16家符合要求,27家整改后符合要求。临床试验项目共抽查5个,检查内容共6个环节72个检查项目。检查情况通报详情内容请查看原文链接。
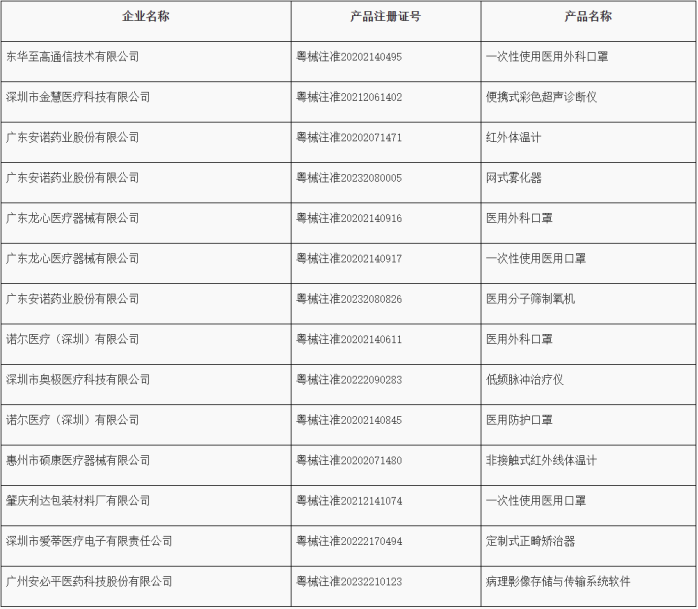
5、广东省药品监督管理局关于同意东华至高通信技术有限公司等10家注册人主动注销《医疗器械注册证》的通告(2024年第105号)
东华至高通信技术有限公司等10家注册人向广东省药品监督管理局主动提出注销产品注册证的申请。根据《医疗器械监督管理条例》的规定,现对该10家注册人持有的14张《医疗器械注册证》依法予以注销(详细内容见原文链接)。

服务赋能 协同创新 | 医疗器械产业质量提升交流会圆满举行
由华测纽唯发起的【广州开发区广州市黄埔区医疗器械行业质量基础设施服务工作站】于2024年5月10日15:00召开了黄埔区医疗器械行业质量提升交流会。
2024-05-20 00:51:42
医疗器械领域再获新突破!| 华测检测CMA扩项获证成功!
2024年2月27日,CTI华测检测有源医疗器械实验室(以下简称“华测医疗器械实验室”)顺利通过国家级CMA资质扩项评审,并已获得资质认定证书及扩项附表。
2024-03-04 00:43:27
CTI华测检测成功入围《深圳市医疗器械优质供应商推荐目录》
深圳市市场监督管理局为贯彻落实深圳市市委、市政府关于产业质量提升的工作部署,着力提升深圳市高端医疗器械产业质量竞争力,推动产业高质量发展,2023年4月11日,深圳市启动了医疗器械产业质量提升“灵渠”计划。
2024-01-22 06:37:44
- 热线电话
- 业务咨询
- 快速询价
- 在线客服
- 报告验证