医械资讯周刊 | 2024年3月第三期
医械资讯周刊,新鲜事简单报,安全用械,共享健康!医械资讯周刊 | 2024年3月第三期,本期要闻:1、国家药监局关于批准注册193个医疗器械产品的公告(2024年2月)(2024年第23号)、2、各省医疗器械许可备案相关信息(截至2024年2月29日)...
1、国家药监局关于批准注册193个医疗器械产品的公告(2024年2月)(2024年第23号)
2024年2月,国家药监局共批准注册医疗器械产品193个。其中,境内第三类医疗器械产品148个,进口第三类医疗器械产品21个,进口第二类医疗器械产品22个,港澳台医疗器械产品2个。
2、各省医疗器械许可备案相关信息(截至2024年2月29日)
为进一步满足企业公众查询医疗器械监管信息的需要,强化社会监督与社会共治,国家药监局汇总了各省(自治区、直辖市)有效期内医疗器械产品注册备案、医疗器械生产企业许可备案、医疗器械经营企业许可备案、医疗器械网络销售备案、医疗器械网络交易服务第三方平台备案信息(附后),按月公布。具体数据可点击国家药监局数据查询页面医疗器械模块查询。
3、器审中心发布创新医疗器械特别审查申请审查结果公示(2024年第3号)
依据国家药品监督管理局《创新医疗器械特别审查程序》(国家药监局2018年第83号公告)要求,创新医疗器械审查办公室组织有关专家对创新医疗器械特别审查申请进行了审查,拟同意以下申请项目进入特别审查程序,现予以公示。
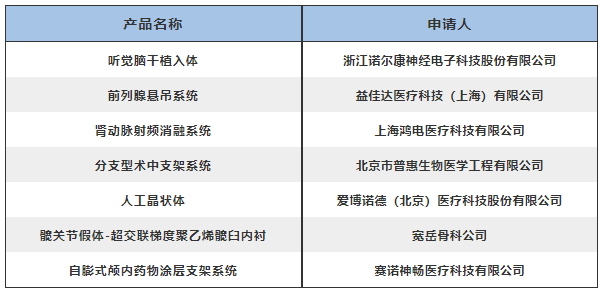
特别说明:进入创新审查程序不代表已认定产品具备可获准注册的安全有效性,申请人仍需按照有关要求开展研发及提出注册申请,药品监督管理部门及相关技术机构将按照早期介入、专人负责、科学审查的原则,在标准不降低、程序不减少的前提下进行审评审批。
4、一次性使用心脏脉冲电场消融导管获批上市
近日,国家药品监督管理局批准了杭州德诺电生理医疗科技有限公司“一次性使用心脏脉冲电场消融导管”创新产品注册申请。该产品由导管和连接电缆组成,与该公司生产的心脏脉冲电场消融仪配合使用,通过控制、释放适当强度的脉冲电场能量,有选择性地仅对需要治疗病灶部位的心肌细胞产生不可逆的电穿孔损伤,从而达到治疗房颤的目的。该产品为药物难治性、复发性、症状性、阵发性房颤的治疗提供了更多选择。药品监督管理部门将加强该产品上市后监管,保护患者用械安全。
5、关于征集参与《人类T淋巴细胞白血病病毒抗体检测试剂注册审查指导原则》等5项体外诊断试剂注册审查指导原则编制工作的相关企业及单位信息的通知
根据2024年指导原则编制计划,为进一步做好相关产品的技术审评工作,器审中心现已启动《人类T淋巴细胞白血病病毒抗体检测试剂注册审查指导原则》、《人类白细胞抗原(HLA)基因DNA分型检测试剂注册审查指导原则》、《人KRAS突变基因检测试剂(PCR法)注册审查指导原则》、《葡萄糖-6-磷酸脱氢酶检测试剂注册审查指导原则》及《酶学检测试剂溯源注册审查指导原则》的编制工作。现征集编制工作参与单位,邀请具有相关工作经验的境内外生产企业、科研机构、临床机构等积极参与。
正式授牌!华测纽唯牵头设立广州市黄埔区医疗器械行业质量基础设施服务工作站
广州开发区质量强区工作领导小组及广州市黄埔区质量强区工作领导小组办公室于2024年3月26日在广州托思北斗创新基地成功举办了“区级质量基础设施服务工作站”授牌仪式!
2024-03-27 16:50:29
医疗器械领域再获新突破!| 华测检测CMA扩项获证成功!
2024年2月27日,CTI华测检测有源医疗器械实验室(以下简称“华测医疗器械实验室”)顺利通过国家级CMA资质扩项评审,并已获得资质认定证书及扩项附表。
2024-03-04 08:43:27
CTI华测检测首登天猫健康专场直播
2021年5月13日-16日,第84届CMEF中国国际医疗器械博览会于上海国家会展中心开幕。作为专业的第三方医疗器械检验检测机构,CTI华测检测在上海国家会展中心设置了展位,与前来参会的行业人员热情交流,并首次登上天猫健康联合聚划算官方推出的“家用器械品类日”专场直播,共同发布电子血压计和电子体温计的推优标准,帮助消费者筛选“更精准”的血压计、体温计,以及使用过程中的注意事项等问题。
2021-05-25 14:34:14
- 热线电话
- 业务咨询
- 快速询价
- 在线客服
- 报告验证