权威丨市场监管总局关于公开征求《在产在售“双无”保健食品集中换证审查要点(征求意见稿)》意见的公告
市场监管总局根据《关于发布〈允许保健食品声称的保健功能目录非营养素补充剂(2023年版)〉及配套文件的公告》(2023年第38号),组织制定了《在产在售“双无”保健食品集中换证审查要点(征求意见稿)》,现面向社会公开征求意见,意见建议反馈截止时间为2024年1月26日。公众可以通过以下途径和方式提出意见建议:
一、登陆市场监管总局网站(网址:http://www.samr.gov.cn),通过首页“互动”栏目中的“征集调查”提出意见。
二、通过电子邮件将意见建议发送至:baojiangongneng cfe-samr.org.cn,邮件主题请注明“《在产在售“双无”保健食品集中换证审查要点(征求意见稿)》公开征集意见”字样。
三、将意见建议邮寄至:国家市场监督管理总局特殊食品司北京市海淀区马甸东路9号,并在信封上注明“《在产在售“双无”保健食品集中换证审查要点(征求意见稿)》公开征集意见”字样。
附件:在产在售“双无”保健食品集中换证审查要点(征求意见稿)






市场监管总局
2023年12月27日
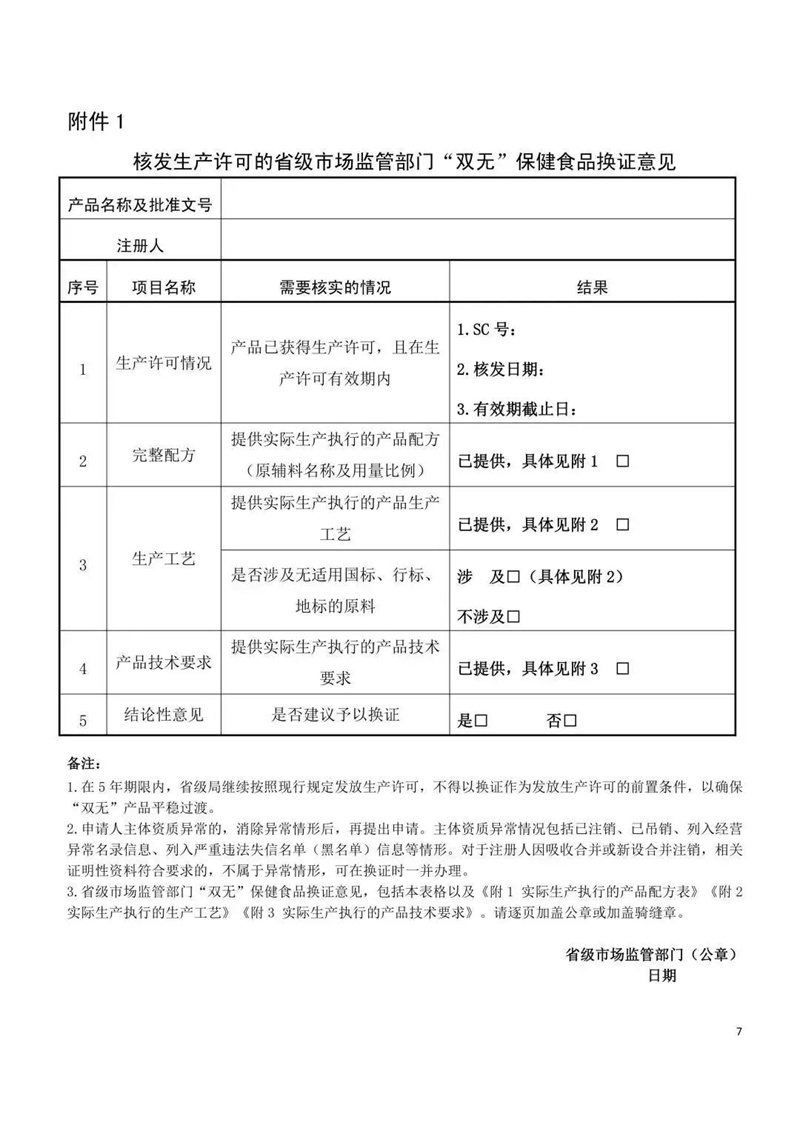
附件一:核发生产许可的省级市场监督部门“双无”保健食品换证意见

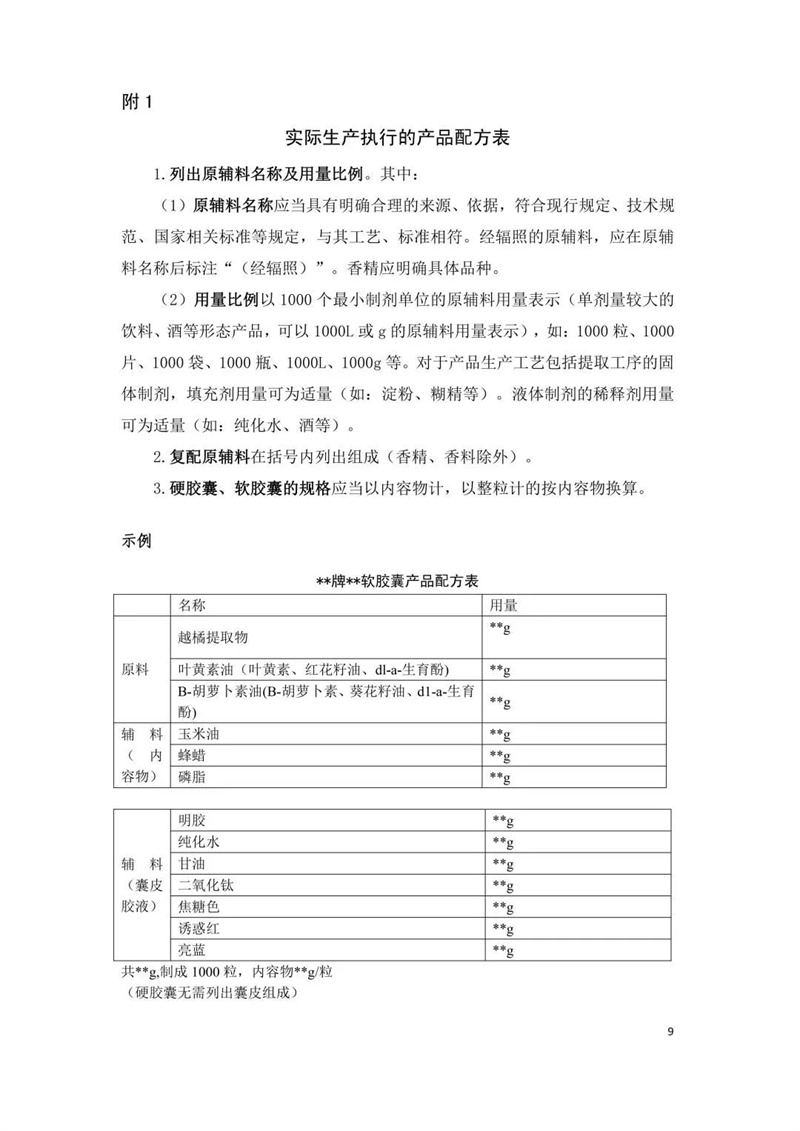

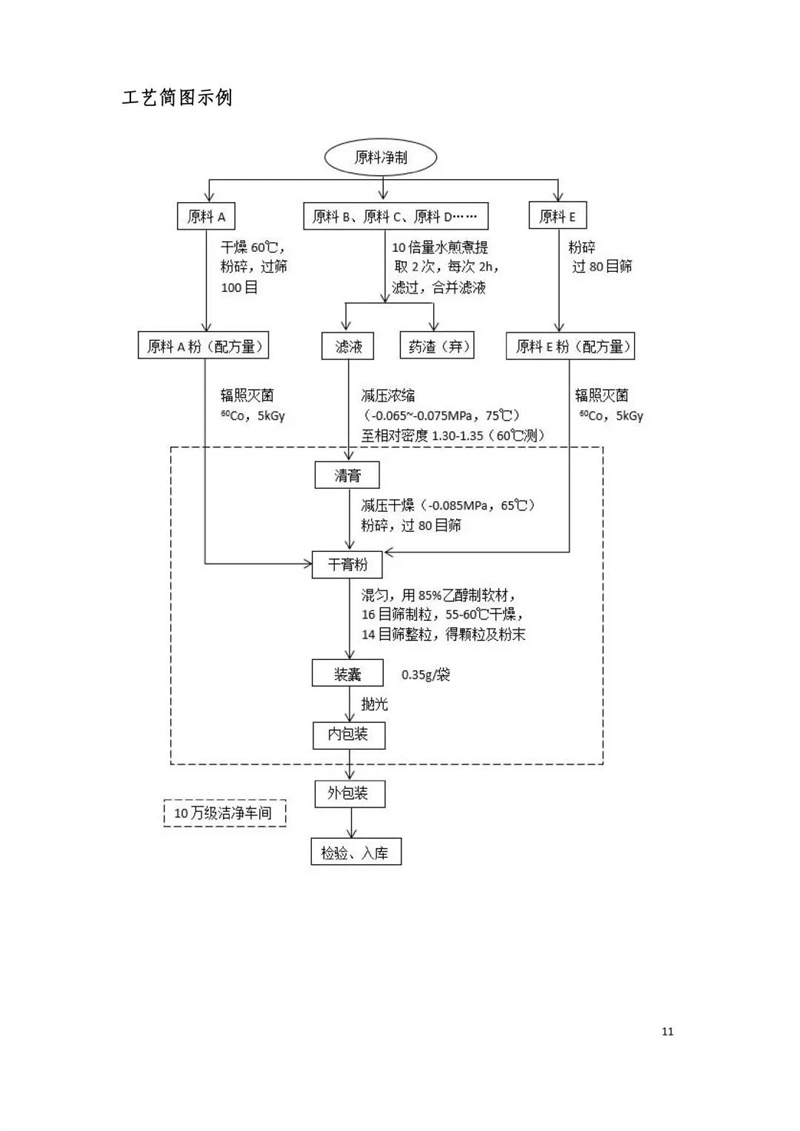






附件二:申请材料目录





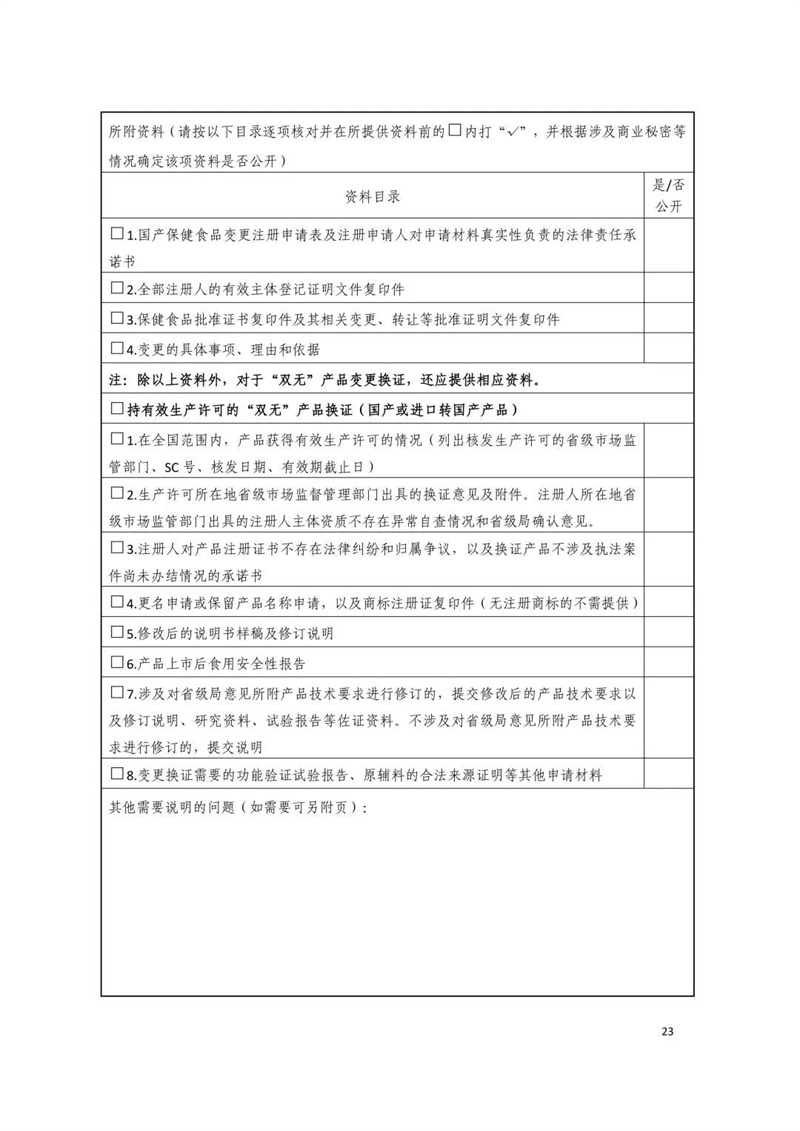



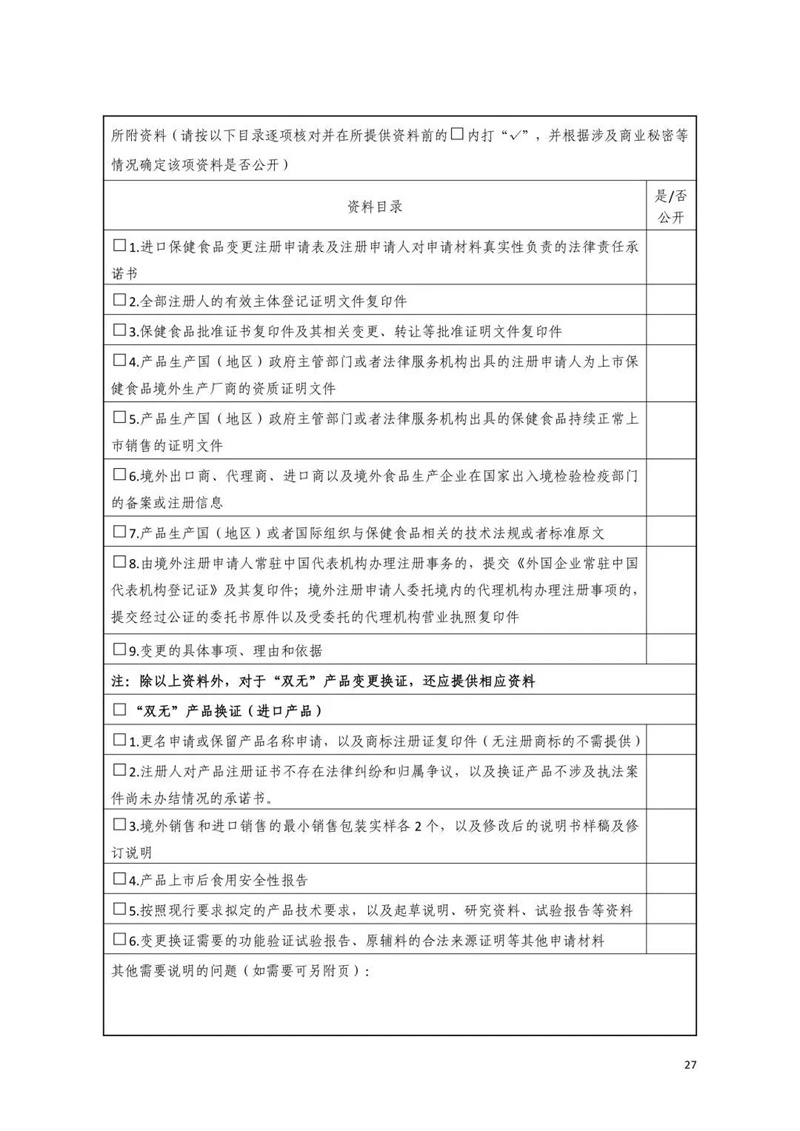
附件三:申请材料要求


CTI华测检测受邀参与“营养保健食品科普知识进社区”公益活动
2024年7月22日下午,为持续开展保健食品科普宣传活动,进一步提升社区群众对保健食品科学认知水平,上海保健品行业协会和普陀区食品药品安全协会联合主办的“保健食品科普知识进社区”公益活动——走进普陀万里社区专场活动,在万里街道党群服务中心顺利举办。
2024-07-31 05:58:04
CTI华测检测与上海保健品行业协会联合举办保健食品法规培训
为帮助会员企业更好的理解并应用新颁布的保健食品法律法规,由上海保健品行业协会主办,CTI华测检测协办的保健食品新规培训于6月5日在上海举办,协会近40家保健食品会员单位参与了本次培训。
2024-06-13 02:09:28
专家解答 | 保健食品原料目录篇
进入保健食品原料目录的原料讨论过的有哪些?对保健食品新功能有什么进展和指导文件么?保健食品原料目录收入了维生素K,为什么功能释义中没有涉及维生素K呢?鱼油备案保健食品用于降血脂,鱼油原料技术要求中,对DHA 与EPA的比例没做限定,EPA含量似与血液低凝固性甚至出血有关,请问DHA与EPA的比例,对降血脂功能有影响吗?
2022-05-16 06:18:08
- 热线电话
- 业务咨询
- 快速询价
- 在线客服
- 报告验证