文献解读 | 代谢流解码肠道菌群与宿主的NAD健康循环
烟酰胺腺嘌呤二核苷酸(NAD)在哺乳动物和微生物中具有重要作用,参与细胞的氧化还原反应与信号转导。NAD+水平的下降与肥胖、炎症、心血管疾病和神经退行性疾病等多种病理状态有关,这种下降通常与线粒体和代谢功能的异常相关,因此近年来NAD+水平的调节成为了研究热点。
本研究旨在探索小鼠肠道微生物群合成NAD的前体物质来源,探索宿主循环中的NAD前体与肠道微生物之间的相互作用,并揭示宿主与肠道微生物之间NAD前体的循环机制。
01研究方法
研究采用8至12周龄的C57BL/6J雄性小鼠开展代谢流实验,通过喂食含有特定同位素标记的NAD前体物质,如U-13C标记的蛋白质、U-13C标记的果糖、2,4,5,6-2H标记的烟酸(NA)和烟酰胺(NAM),来追踪NAD前体物质在宿主和肠道微生物中的代谢路径。
代谢流分析测量标记的NAD前体物质在宿主和肠道微生物中的分布和转化,定量分析NAD的生物合成途径。
为确定肠道微生物在NAD前体物质代谢中的作用,以多种抗生素耗竭小鼠肠道中的微生物群落,并比较经抗生素处理和未经处理小鼠的NAD前体物质代谢情况。
代谢组学分析采集小鼠血液等相关样本,使用液相色谱-质谱联用(LC-MS)技术来定量分析测量标记的NAD前体物质和NAD产物的浓度。
02研究结果
本研究揭示了肠道微生物与宿主之间NAD前体物质的循环机制,发现了宿主循环中的烟酰胺(NAM)是肠道微生物合成NAD的主要来源,而非直接来自食物的NAD前体。
代谢流检测证实,宿主来源的NAM进入肠道后,被微生物转化为烟酸(NA),这一过程绕过了宿主的NAD合成挽救途径,直接支持了宿主组织中的NAD合成。
研究发现,口服烟酰胺核糖苷(NR)主要通过肠道微生物转化为NA,进而提高宿主组织中的NAD水平;可溶性纤维如菊粉在大肠中对微生物NAD合成有重要贡献,而简单糖类如果糖在过量摄入时也能在结肠中支持NAD合成。
在抗生素处理后,小鼠肠道微生物群的耗竭显著影响了NAD前体物质的代谢,从而证实了肠道微生物在NAD代谢中的关键作用。
03研究结论
研究发现,宿主来源的NAM对肠道微生物NAD合成的贡献显著高于食物中的直接NAD前体,NR主要通过肠道微生物转化为NA,进而促进宿主组织NAD的合成。
这些结果提供了新的视角,通过调节宿主与肠道微生物间的关系,或有助于改善代谢健康,预防治疗多种与NAD水平下降相关的疾病。
04研究结果展开
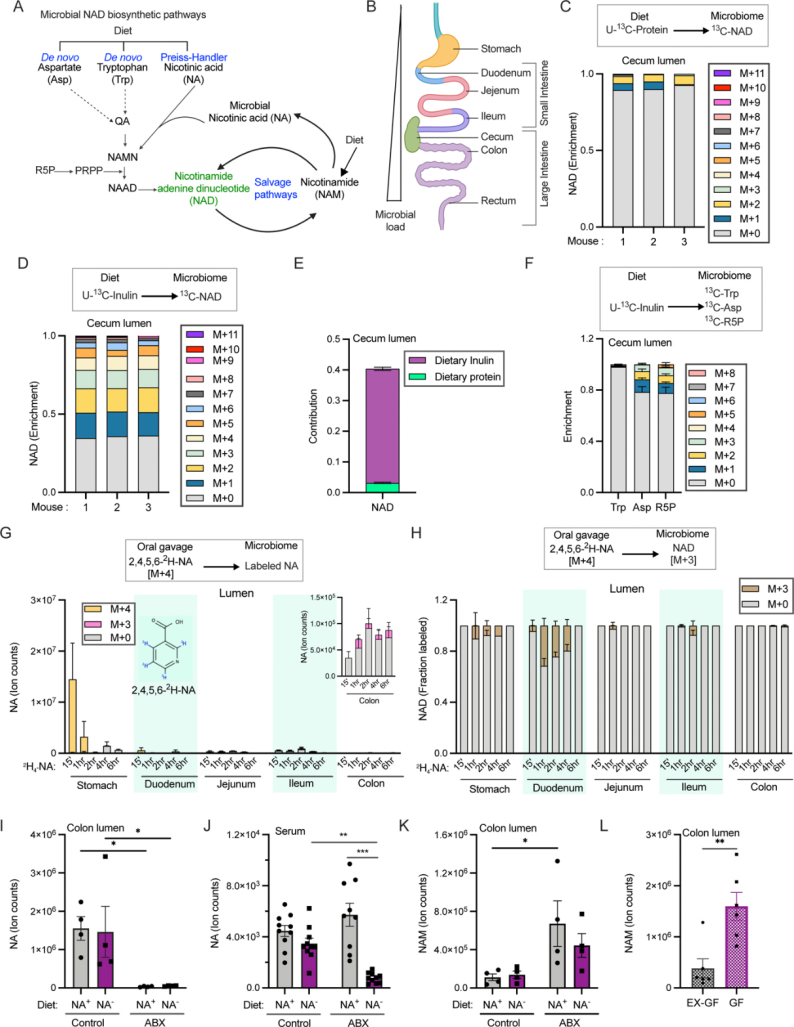
图1.显示了微生物NAD合成的代谢途径不能仅通过饮食前体来解释
A.展示了微生物中NAD合成的详细途径,包括烟酸(QA)、烟酸单核苷酸(NAMN)和烟酸腺嘌呤二核苷酸(NAAD)等关键中间产物。B.展示了小鼠消化道的不同部分。C.显示了小鼠喂食U-13C标记的蛋白质24小时后,盲肠中NAD出现了富集。D.显示了小鼠喂食含有U-13C标记的菊粉24小时后,盲肠中NAD出现了富集,且贡献更为显著。E.定量分析U-13C标记的蛋白质和菊粉对盲肠中NAD合成的影响。F.显示菊粉代谢中间产物的富集情况,包括色氨酸、天冬氨酸和核糖磷酸。G.显示口服标记烟酸在肠道的代谢分布主要在结肠被微生物转化为NAD。H.对比了肠道不同部位NAD标记以显示饮食前体在微生物NAD合成中的作用。I.显示含或不含烟酸饮食以及抗生素处理对小鼠结肠中NA含量的影响。J.显示含或不含烟酸饮食以及抗生素处理对小鼠血清中NA离子计数的影响。K.显示含或不含烟酸饮食以及抗生素处理对小鼠结肠中NAM含量的影响。L.对比了无菌小鼠和菌群定植小鼠结肠中NAM丰度,显示菌群在NAD代谢中的重要性。
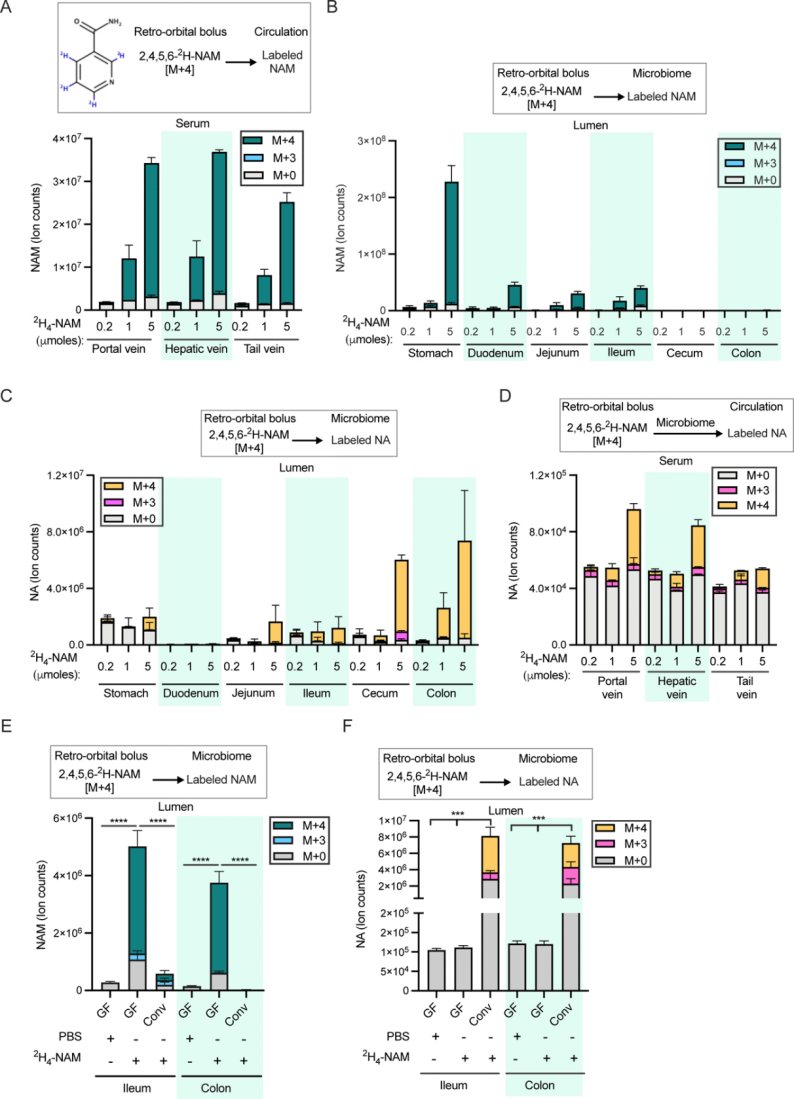
图2.展示血液循环中的NAM进入肠道菌群NAD合成
A.通过眼眶后注射不同剂量的[2,4,5,6-2H]-NAM后15分钟,收集门静脉、肝静脉和尾静脉血清样本中的NAM水平。B.通过眼眶后注射不同剂量的[2,4,5,6-2H]-NAM后,小鼠肠道检测到的标记NAM。C.通过眼眶后注射不同剂量的[2,4,5,6-2H]-NAM后,不同部位消化道样本中NA。D.通过眼眶后注射不同剂量的[2,4,5,6-2H]-NAM后,血清样本中NA。E.通过眼眶后注射不同[2,4,5,6-2H]-NAM后,比较无菌小鼠和对照小鼠肠道中NAM。F.通过眼眶后注射不同[2,4,5,6-2H]-NAM后,比较无菌小鼠和对照小鼠肠道中NA。
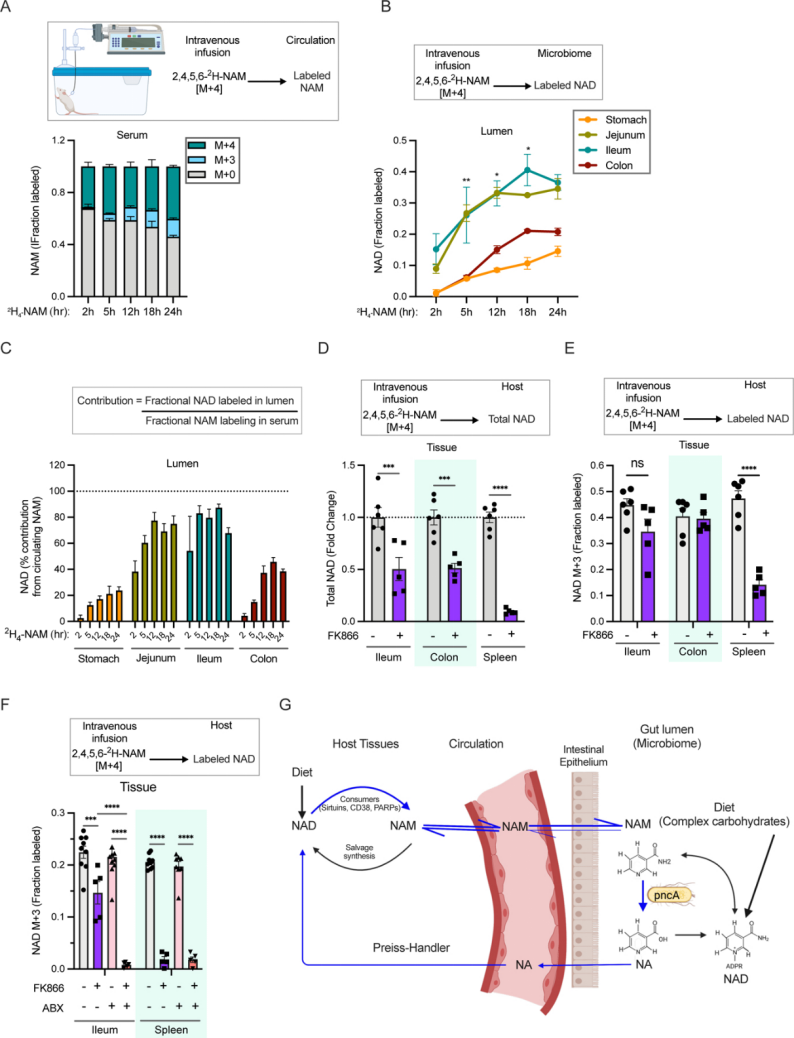
图3.维生素B3在宿主和肠道微生物群之间的循环
A.小鼠被灌注[2,4,5,6-2H]-NAM后血清中烟酰胺变化。B.小鼠被灌注[2,4,5,6-2H]-NAM后肠道中NAD变化。C.小鼠被灌注[2,4,5,6-2H]-NAM后血液中NAM对消化道NAD合成的贡献。D.小鼠先腹腔注射FK866(NAMPT抑制剂),再灌注[2,4,5,6-2H]-NAM后NAD的相对水平。E.小鼠先腹腔注射FK866(NAMPT抑制剂),再灌注[2,4,5,6-2H]-NAM后标记的NAD比例。F.从小鼠收集的组织中标记的NAD比例,对比分析小鼠接受抗生素(ABX)处理,腹腔注射FK866,灌注[2,4,5,6-2H]-NAM后组织中标记NAD比例。G.卡通图显示宿主和肠道菌群间维生素B3循环。宿主血液中NAM进入肠道,被菌群去氨基化成NA;宿主使用菌群产生的NA来合成NAD,而NAD的转化又释放出NAM。
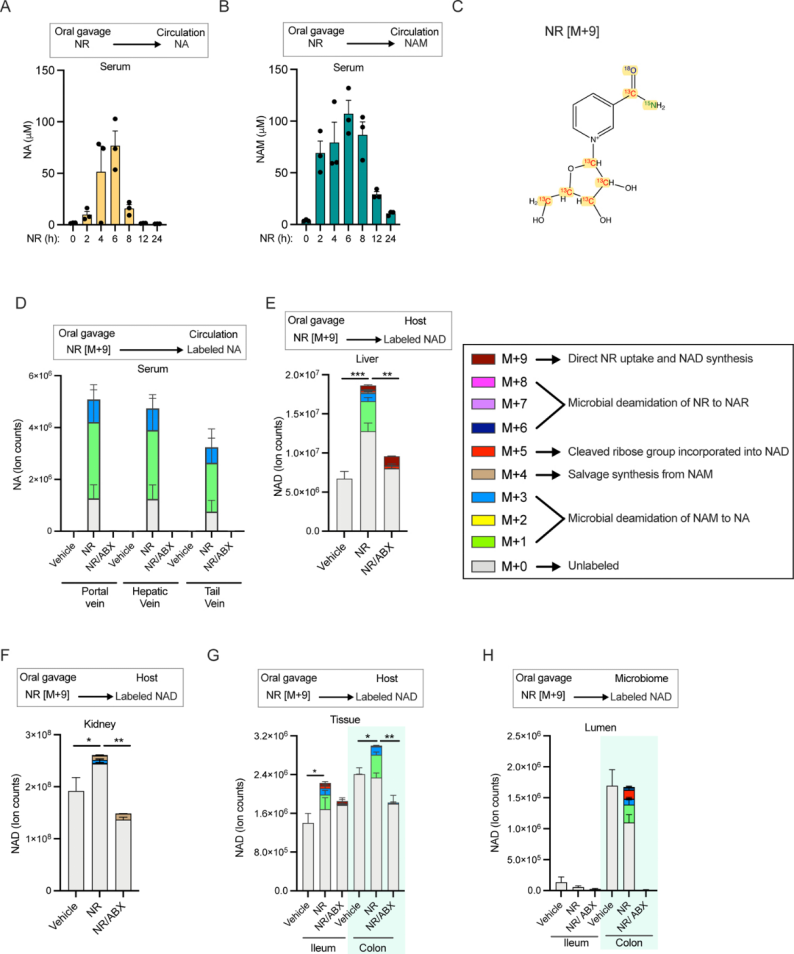
图4.展示了口服NR(烟酰胺核糖苷)通过肠道转化为NA(烟酸)来增加宿主NAD合成
A.小鼠口服NR后测定血清中NA浓度。B.小鼠口服NR后测定血清中NAM(烟酰胺)浓度。C.展示M+9 NR的同位素标记示意图,烟酰胺部分用15N、13C和18O进行标记,核糖环上用13C碳标记。D.对比抗生素(ABX)处理过的小鼠在口服NR后血清中NA的相对水平。E.对比抗生素(ABX)处理过的小鼠在口服NR后肝脏中NAD水平。F.对比抗生素(ABX)处理过的小鼠在口服NR后肾脏中NAD水平。G.对比抗生素(ABX)处理过的小鼠在口服NR后肠道组织中NAD水平。H.对比抗生素(ABX)处理过的小鼠在口服NR后肠道中NAD标记模式。
05总结与启发
该篇文献发表于Cell Metab.(IF>27),研究使用代谢流技术,追踪了NAD在宿主和肠道菌群中的代谢变化,揭示了宿主血液中NAM对菌群合成NAD的贡献,充分展示了代谢流技术在解析复杂生物系统中物质转换和代谢途径中的重要作用。
研究的一个亮点在于探讨了NAD合成途径的调控机制,为理解NAD代谢在疾病中的作用提供了新的视角。
研究中数据呈现和图表排列清晰、逻辑性强,逐步展示了NAD前体的代谢路径、宿主与微生物间的代谢循环,以及NR在宿主组织中的作用,使得复杂的代谢过程变得易于理解,也突出了研究的主要发现和结论。
因此这项研究提供了一个代谢流技术应用的例子,成功揭示了NAD代谢在宿主健康和疾病中的潜在作用,为未来的研究和临床应用奠定了坚实的基础。
参考文献
Chellappa K,McReynolds MR,Lu W,Zeng X,Makarov M,Hayat F,Mukherjee S,Bhat YR,Lingala SR,Shima RT,Descamps HC,Cox T,Ji L,Jankowski C,Chu Q,Davidson SM,Thaiss CA,Migaud ME,Rabinowitz JD,Baur JA.NAD precursors cycle between host tissues and the gut microbiome.Cell Metab.2022 Dec 6;34(12):1947-1959.e5.doi:10.1016/j.cmet.2022.11.004.PMID:36476934;PMCID:PMC9825113.
华测多组学科研服务AI+靶向代谢组学智能临床转化平台亮相第二届多组学科研大会
2024年3月30日至31日,第二届多组学科研与临床应用大会在上海丽昂豪生大酒店盛大开幕,大会以“聚焦多组学,从科研到临床”为主题,吸引了国内外众多专家学者相关的基础研究、临床应用、产业从业者参与,全场座无虚席。
2024-04-02 00:59:15
柿子变身记:这个冬天,“柿柿”如意
CTI华测检测可为您提供柿子等新鲜果蔬的营养品质、农药残留、产地环境等检测套餐服务。我们拥有专业的技术支持团队与一流的检测团队,为食品安全保驾护航。
2021-12-22 09:02:36
CTI华测检测开通深圳地区数字证书业务
随着2021深圳全球招商大会举行,当前深圳进入了“双区”驱动、“双区”叠加的黄金发展期,国际一流营商环境催生了377万户商事主体。近日,华测CA顺应市场所需助力网上商事登记,在深圳已推出个人数字证书业务,ODC组织机构数字证书业务也即将上线。
2021-12-20 06:06:12
- 热线电话
- 业务咨询
- 快速询价
- 在线客服
- 报告验证