交叉参照,让数据说话!你一定要知道的化妆品安全评估知识
一、引言
交叉参照(Read-across)是一种基于化学结构或生物学活性相似性,通过利用一种或多种类似化学物质的毒理学终点数据来预测另一种或一类结构相似的特定化学物质的相同毒理学终点信息的方法。该方法在化学品安全评估中扮演着重要角色,特别是在缺乏直接测试数据的情况下。本文将详细介绍交叉参照方法的发展历史、法规进程、主要工具及类型以及举例说明。
二、发展历史
交叉参照方法的起源可以追溯到科学研究的早期,但其在化学品安全评估中的广泛应用则始于近几十年。随着化学品数量的快速增长和环保意识的增强,传统的试验方法因成本高、耗时长等缺陷而难以满足需求。因此,科学家们开始探索利用已有数据来预测新化学物质的安全性的方法,交叉参照便应运而生。
三、法规进程

四、主要工具
交叉参照过程中,通常需要使用一种或多种工具来辅助识别类似物和预测目标化学物质的毒性。以下是一些常用的工具:
OECD QSARToolbox:由经济合作与发展组织(OECD)开发的工具箱,提供了一系列用于交叉参照的模型和工具。
EPA CompTox Chemicals Dashboard:美国环保署的化学品数据库和工具,其中的GenRA模型可用于交叉参照分析。
Toxtree:一个免费的软件工具,可基于化学结构初步筛选类似物,但不能直接代替交叉参照过程。
此外,还有一些商业软件和服务提供商也提供交叉参照相关的解决方案。
五、交叉参照的原理及前提
交叉参照是用源化学物质信息来预测目标化学物质相同终点的信息。前提是基于源化学物质和目标化学物质应该“相似”。
1.结构相似性
- 相同的功能基团(例如:醛类,环氧化物,酯类等)
- 类别物有规律的变化(例如:碳链长度变化类别)
- 相同的组分或化学类别,类似的碳原子数目(例如:UVCBs)
- 通过物理或生物过程产生的结构相同或相似的前体或分解产物(例如:酸/酯/盐的通过代谢途径产生相同或相似的化学物质;例如:甲酸丙酯和甲酸异丁酯的水解产物是类似的)
2.机制相似性
作用机制是造成不良影响的原因及生物化学过程
-可以用于确定NOEL,例如DART,慢性毒性
-可用AOP来定义
通过确认目标和源分子通过相同的作用机制起作用,可以确保交叉参照的可靠性。
(某些特定的官能团如醛基、羧基、酰胺基等,在特定条件下可能引发机体的免疫反应。)
六、交叉参照类型
交叉参照方法主要分为两类:类似物法和类别法。
1. 类似物法
类似物法基于目标化学物质与一个或多个源化学物质的相似性进行交叉参照。这些相似性可能包括相同的官能团、相似的化学结构、相同的代谢途径和生物反应性等。通过比较目标化学物质和源化学物质的毒理学数据,可以预测目标化学物质的毒性。
2. 类别法
类别法则是在化学物质分组的基础上进行交叉参照。首先,将具有相似结构、理化性质或毒理学特性的化学物质分组,然后利用组内已知化学物质的毒性数据来预测组内其他化学物质的毒性。这种方法适用于大量化学物质的快速评估。
七、交叉参照的步骤
1.收集和整理目标化学物质的信息:包括结构信息、理化性质、毒理学数据、代谢途径和代谢产物等。
2.确定数据缺口:根据已收集到的信息,明确需要预测的毒理学终点。
3.识别与确定潜在的类似物:基于化学结构、代谢途径和生物反应性等相似性,识别与目标化学物质具有潜在相似性的类似物。国际权威机构通常会根据化合物的类别,对一组化合物进行安全评估,如果目标化合物属于某个分组评估,或者在结构、物理化学、生物学和毒理学性质上与被评估的化学物分组表现出相似性,那么就可以通过权威审查来进行交叉参照。
常见权威机构包括:CIR、SCCS、RIFM、OECD、WHO、US EPA、AICIS、Health Canada、Etc.
4.收集源化学物质/参考化学物质数据:收集并整理源化学物质的理化性质和毒理学数据。
通常可以通过多种软件进行相似性的搜索,示例如下:
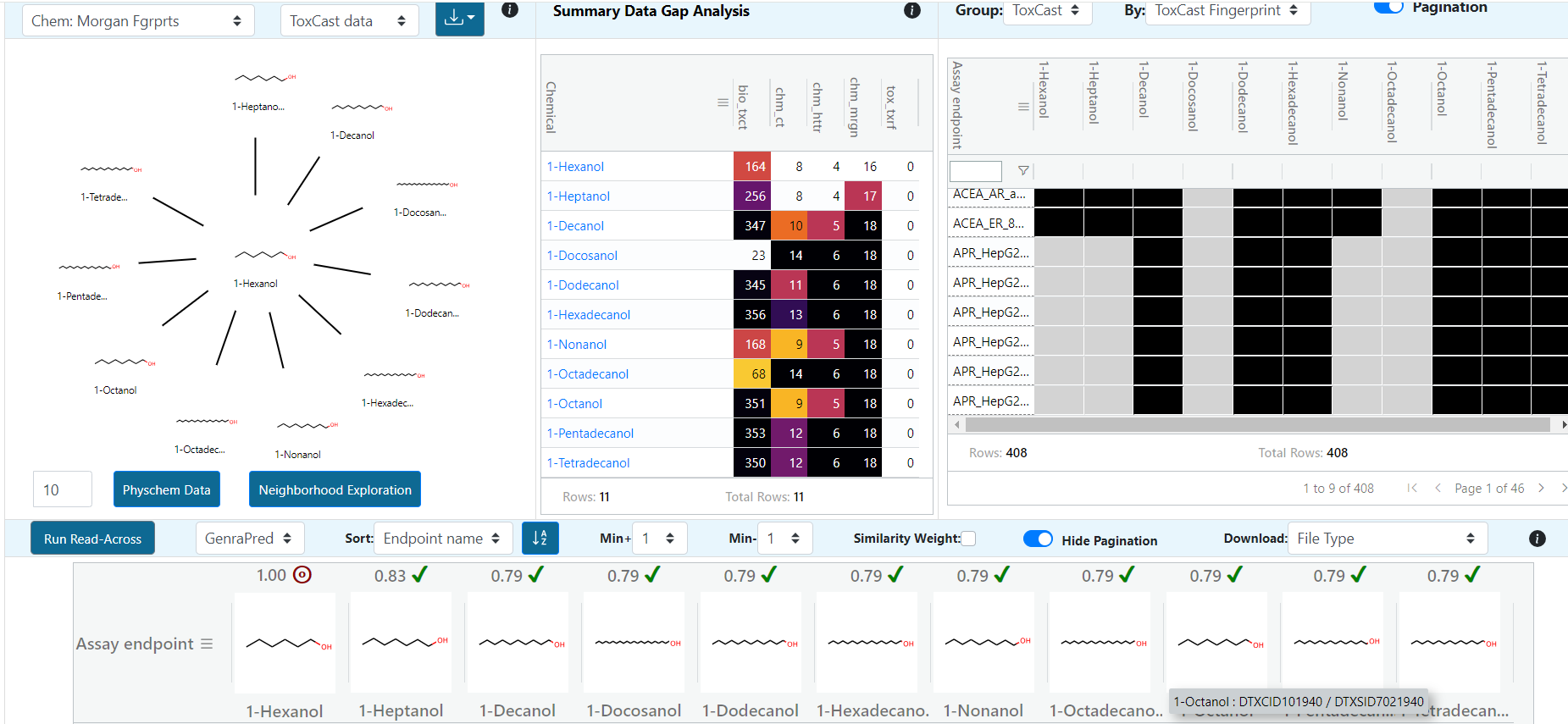
5.收集源头化学物质数据并确定选用类似物法或类别法
通过软件筛选出类似物后,不能单独根据相似性系数来评估相似性,还需要结合化合物的化学结构、反应性、代谢和理化性质进行相似性判断。(通常来说,可以通过PubChem去查询化合物的性质,PubChem是美国国立卫生研究院(NIH)下属的国立生物技术信息中心(NCBI)维护的一个免费的化学结构数据库)。
如果有较多类似物,可以采取化学物分组。通过进一步细分来判别类别是否成立,从而降低数据集的不确定性,从而去除可能与目标化合物在机理或代谢等方面有不同的类似物,记录选择或排除 潜在类似物的理由。
数据的收集可以是多途径的(例如研究报告,公开发表的论文,数据库等)
6.构建数据矩阵表,进行数据缺口评估与分析
通过对收集到的数据进行进一步整理,从而判断现有数据能否支撑对于目标化合物缺少毒理学数据的填充。对目标化合物的物理化学性质及毒理学终点构建数据矩阵。如果现有数据不足以填充目标化合物毒理学空白或数据缺乏可靠性和关联性,则需要收集其他数据进行数据缺口填补。
7.验证交叉参照的可靠性、相关性和充分性评估:可靠性在于评估用来填补数据缺口的数据是否可靠,来源是否权威;相关性在于评估数据和测试在多大程度上适用于特定的危害识别和风险表征;充分性在于数据对于危害/风险评估的有用性和完整性。(可靠性评分过程参考ECVAM的ToxRTool)
8.验证交叉参照的合理性和不确定性评估:通过比较目标化学物质和源化学物质的相似性,验证交叉参照的合理性,并评估可能存在的不确定性。
合理性可以通过以下途径但不局限:物理化学性质、毒代动力学、作用模式等;相似性的验证:
如果是有相似机构的就需要验证相似结构;
如果是代谢过程类似,就需要验证有相同的代谢产物等;
建立数据矩阵,对数据进行相似性比较评估,如果使用的是类别法,则需要评估各终点的变化规律。
9.填补数据缺口:如果确认了交叉参照的合理性,且来源数据真实可靠,那么就可以通过交叉参照方法对目标化合物的数据缺口进行填充,并分析交叉参照可能存在的不确定性对交叉参照的影响,对最后的数据选择合理性进行说明。
10.形成评估报告:报告应该包括的要素,目标化合物和类似化合物的化学特征描述、支持交叉参照的假设、目标化合物和类似化合物之间的结构和/或机制的相似性的验证、目标化合物和类似化学物的数据矩阵。
八、结论
交叉参照作为一种非测试方法,在化学品安全评估中发挥着重要作用。通过合理利用现有数据,可以有效减少测试需求,提高评估效率。然而,交叉参照方法的准确性和可靠性也取决于数据的质量和相似性假设的合理性。因此,在使用交叉参照方法时,需要严格遵循相关法规和指南,确保评估结果的科学性和可靠性。
CTI华测检测携手扬州市化妆品协会举办国产普通化妆品备案培训
2024年8月8日-9日,为贯彻落实国家和省药监部门关于做好化妆品相关工作的通知要求,进一步提升扬州市化妆品备案质效,扬州市市场监管局联合省药监局扬州检查分局、扬州市化妆品协会组织开展了2024年第一轮国产普通化妆品备案培训。全市化妆品生产企业代表等共计百余人参加培训。
2024-08-23 03:50:40
直播邀请 | 儿童化妆品法规解读及监管趋势洞察
为规范儿童化妆品生产经营活动,加强儿童化妆品监督管理,保障儿童使用化妆品安全,2021年10月08日,国家药品监督管理局发布《儿童化妆品监督管理规定》(2021年第123号公告)。这是我国首个专门针对儿童化妆品的法规,意味着儿童化妆品迎来“独立监管”时代,此次的《规定》较一般化妆品更为严格的监管要求。2022年4月11日,中检院再次发布《儿童化妆品技术指导原则》(征求意见稿),进一步明确儿童化妆品的监管要求,分别对企业产品研发、技术评审及备案提出了相关指导及依据。
2022-05-18 04:10:07
国家药监局 | 化妆品新原料注册备案管理政策问答
依据《化妆品监督管理条例》(以下简称《条例》)、《化妆品注册备案管理办法》(以下简称《办法》)和《化妆品新原料注册备案资料管理规定》(以下简称《规定》),国家药监局化妆品监管司收集、整理了化妆品业界比较关注的化妆品新原料注册备案相关问题,并逐一进行了解
2021-11-16 23:26:48
- 热线电话
- 业务咨询
- 快速询价
- 在线客服
- 报告验证